Gestion des pharmacies hospitalières
Gamme sanitaire hors MCO
Optimisez votre gestion économique et financière tout en sécurisant votre circuit du médicament

Osipharm est une solution :
- Ouverte et communicante
- Eprouvée (plus de 650 Finess équipés)
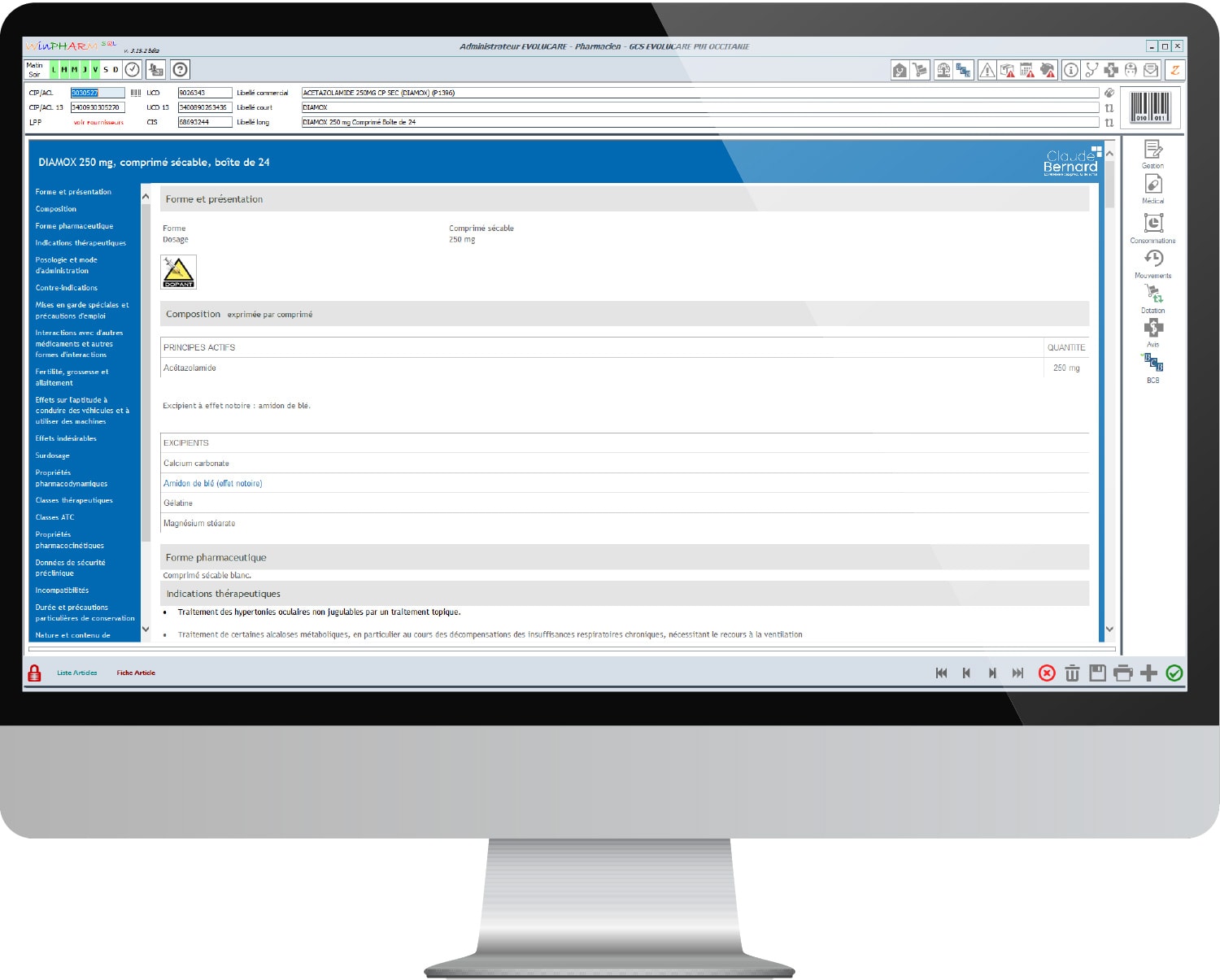
- Gestion économique et financière des P.U.I.
- Référentiel produit avec mises à jour régulières
- Gestion assistée des achats et commandes
- Lecteur de code-barres (achats, inventaires et sorties de stocks)
- Ergonomique, intuitif et paramétrable
- Alertes sur retraits de lots, ruptures, ATU…
- Gestion de la sérialisation
Sérialisation
Respect de la règlementation :
- Agrément de notre solution par France MVO
- Historisation des actions réalisées
- Traçabilité des échanges
Lecture des codes-barres optimisée :
- Scan unitaire (boîte par boîte)
- Scan au conditionnement (palette, carton, …)
- Lecteurs autonomes ou filaire (voir image)
Consulter l’article “Osipharm et Winpharm prêts pour la sérialisation” (02/2019)

Interopérabilité
- Livret thérapeutique

- Intégration des prescriptions
- Retour/validation pharmaceutique
- Traçabilité des dispensations
Formats propriétaires – Comptabilité générale & analytique :
- Transfert des factures / avoirs
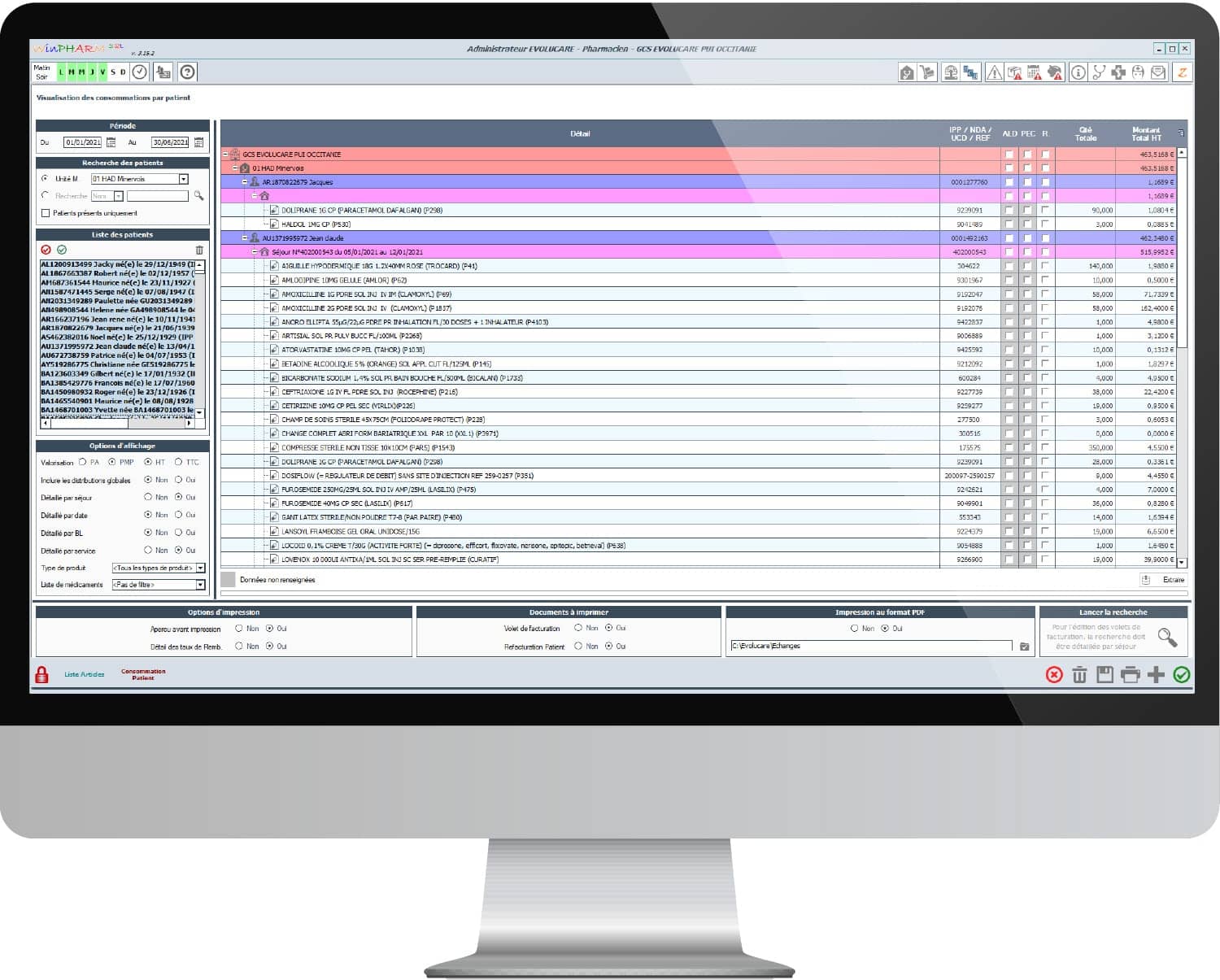
- Transfert des consommations par UF
- Transfert des variations de stock
- Intégration des identités

- Intégration des séjours/mouvements
- Transfert en facturation des UCD et LPPr
Lien avec les centrales d’achats (CACIC, CAHPP, Helpévia) :
- Intégration des catalogues
- Mise a jour automatique des prix tarifs
- Sécurisation de vos commandes via l’EDI
+30
ans d’expertise
+650
clients
+350 000
commandes EDI / an
Osipharm en détail
Gestion des livrets
- Multi livrets
- Spécialisation (Livret thérapeutique, DM, Livret par spécialité)
- Hiérarchisation (Groupe, Etablissement)
Référentiel produits
- Nouveau bus inter applicatif web
- Interopérabilité avec le noyau commun Serveur de Produits
- Supervision des référentiels produits par un super-administrateur
- BCB
- VIDAL
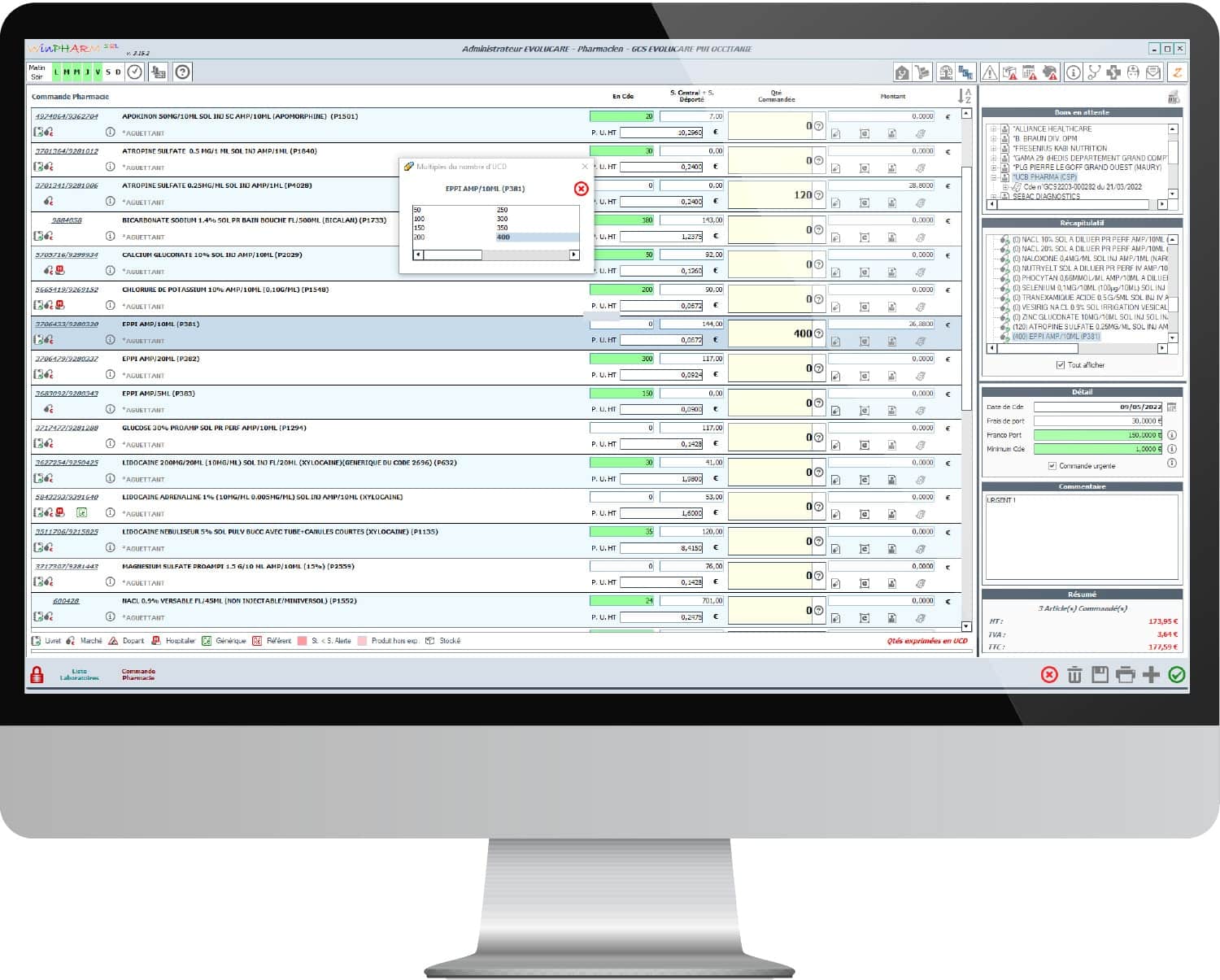
Gestion des achats
- Préparation automatique des commandes
- Saisie des commandes assistées
- Préparation des commandes par lecteur code-barres
- Transfert des commandes par EDI et par courriel
- Saisie facilitée des réceptions et des factures
- Interfaces comptables
- Gestion multi fournisseurs
Gestion des alertes
- Alertes paramétrables par utilisateur
- Besoins en réapprovisionnement
- Articles en péremption
- Stocks dormant
- Messages
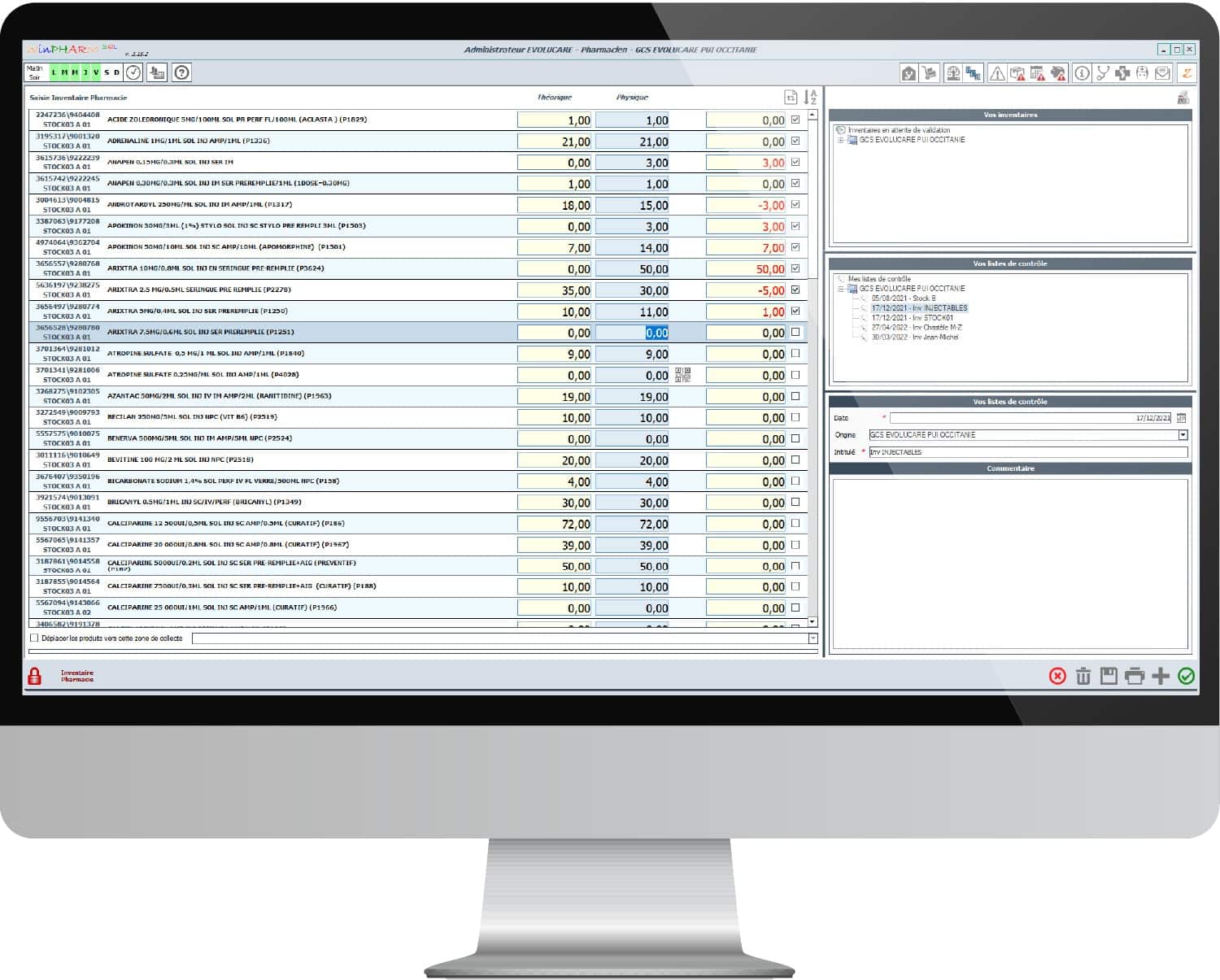
Gestion des inventaires
- Pharmacie
- Etages
- Stocks déportés
- Multi-valorisation
Gestion des multi sites et des unités de stocks déportées
- PUI en GCS (Groupement Coopératif Sanitaire)
- Groupe mutualisé avec reporting régional et/ou national
- Sites intermédiaires de stock, etc.
Enquêtes de suivi d’activité de la PUI
- Nationales auprès des tutelles (DREES, SAE, spécifiques, etc.)
- Ration d’optimisation des stocks, des consommations, achats
- Hit-parade par classe ATC, CLADIMED, … en volume et en valeur
- Suivi budgétaire par site ou multi sites